服务热线
13618350705
 当前位置:首页
> 新闻资讯
当前位置:首页
> 新闻资讯 
近年来,越来越多的疑难杂症最终被诊断为自身免疾性疾病,自身免疾性疾病的发病率逐年升高。自身免疾性疾病的致病机制复杂,可累及多器官、多系统。其病种繁多,临床表现复杂多样,且发病隐匿,诊治困难。
目前,对于自身免疾性疾病的诊疗,自身抗体检测对自身免疾性疾病的预测、诊断和治疗等均至关重要,给临床提供了很多诊疗依据。
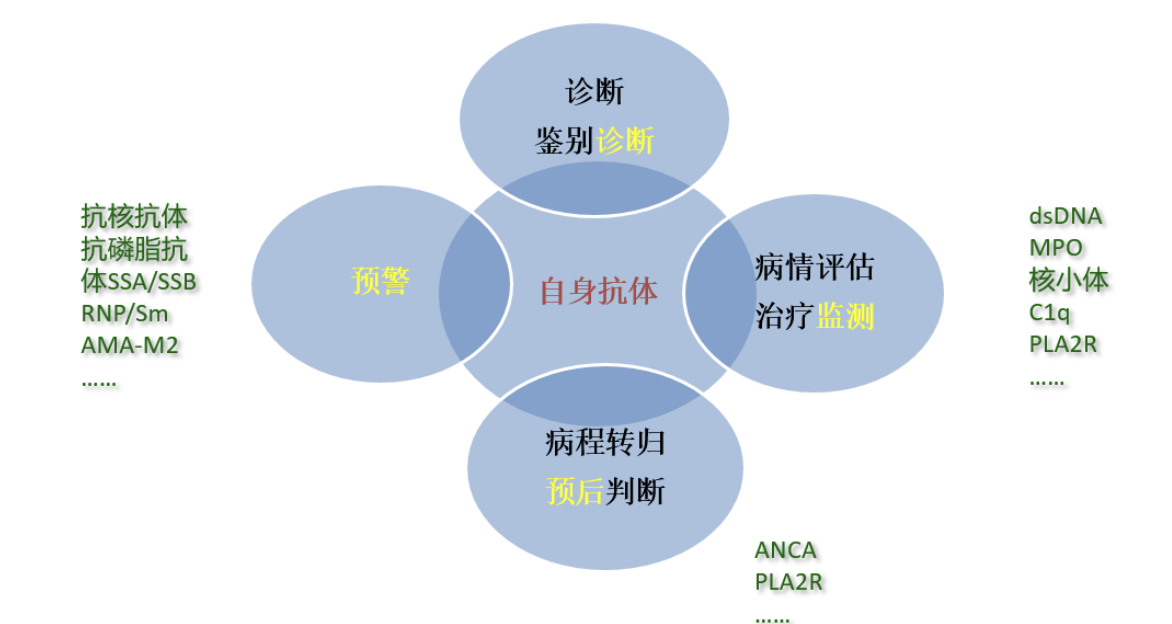
其中,部分自身抗体与病情评估、疾病活动度、预后等密切相关,有随访监测的价值。比如,相关研究和指南均指出ANA、ANCA中多种特异性抗体的滴度水平与疾病严重程度、活动度、预后等相关,对随访监测和药物的使用有指导意义。如,抗双链DNA(dsDNA)抗体、抗核小体抗体的滴度水平与疾病活动度相关,抗髓过氧化物酶(MPO)抗体的滴度水平与肾小球新月体形成数目及疾病活动度相关。抗环瓜氨酸肽(CCP)抗体阳性者且随着滴度水平的升高,通常会出现或易发展成更为严重的关节骨质破坏。在系统性红斑狼疮(SLE)患者血清中,持续性中高滴度水平的抗心磷脂(aCL)抗体可大大增加血栓的风险。抗ß2糖蛋白1(β2 GP1)抗体与血栓发生的相关性与抗aCL抗体相仿。抗磷脂酶A2受体(PLA2R)抗体检测有助于监测疾病的进展与转归、评估疾病风险分层、决策全程个体化治疗等。因此,部分诊断/分类标准中根据某些自身抗体水平的高低赋予了不同的权重。综上,可以发现,自身抗体的部分指标确实不仅要检测阴阳性,对他们的定量检测也很重要。
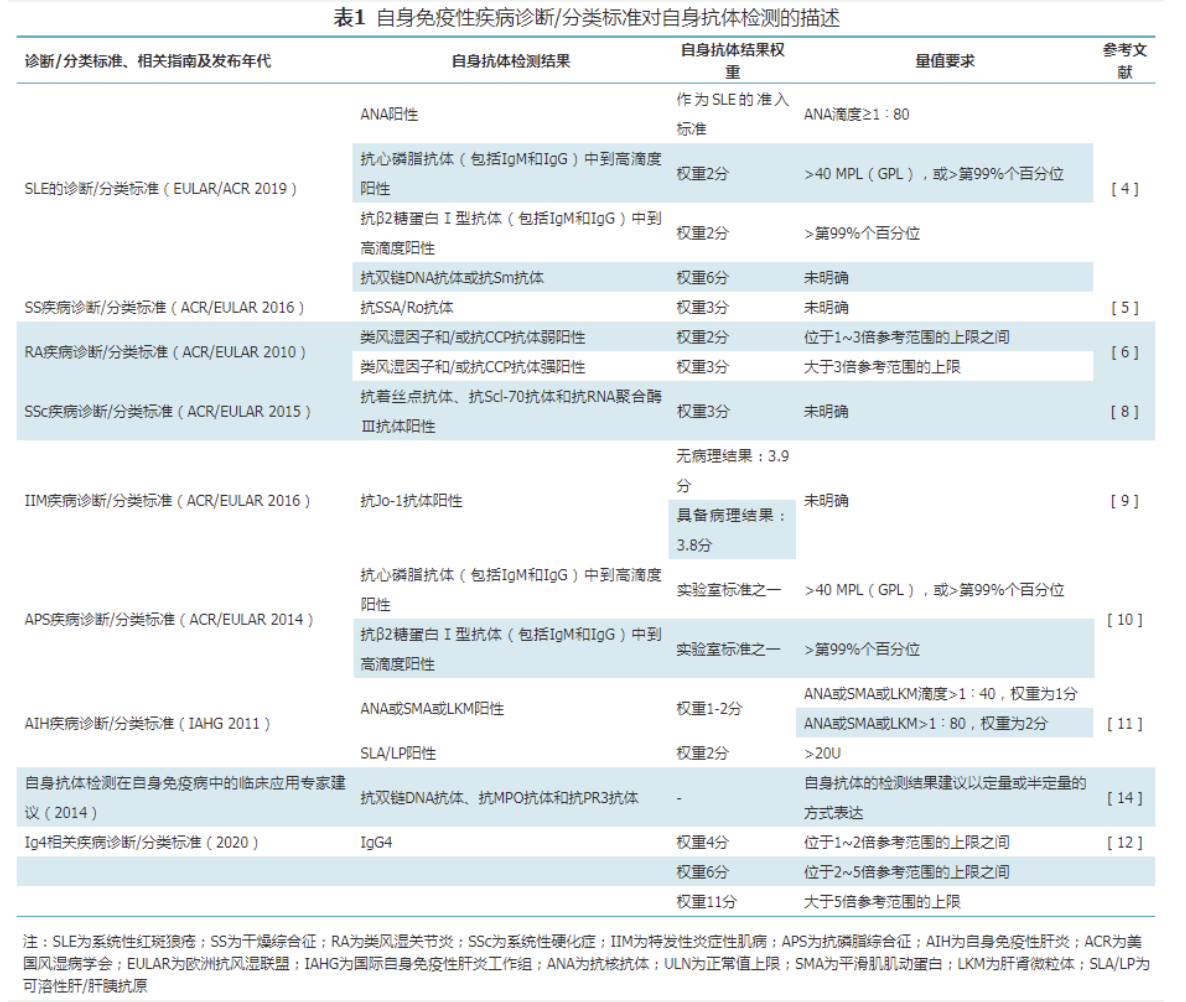
但是,自身免疾性疾病通常具有独特的疾病特点,比如一种疾病对应多种自身抗体,一种自身抗体又会出现在多种疾病中,不同疾病相关自身抗体间又多有重叠等。因此,对于自身免疾性疾病,“抗体谱”的检测不可忽视。综上,除少数自身抗体外(如dsDNA、CCP、MPO、PR3、aCL、β2 GP1和PLA2R等)。其实,多数自身抗体的滴度水平与疾病的严重程度、病程分期、预后等可能没有非常相关的指导关系。是否需要全面升级到“全定量“水平,如何选择自身抗体的检测方法,还应结合实验室自身的实际需求来确定。
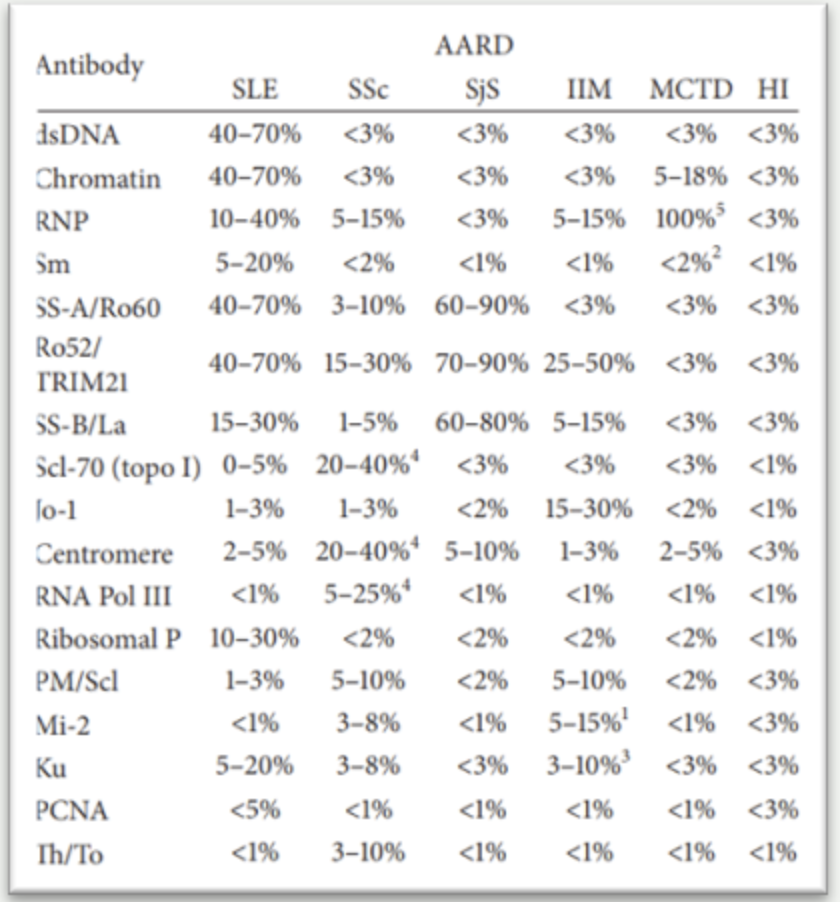
J Immunol Res. 2014;2014:315179.
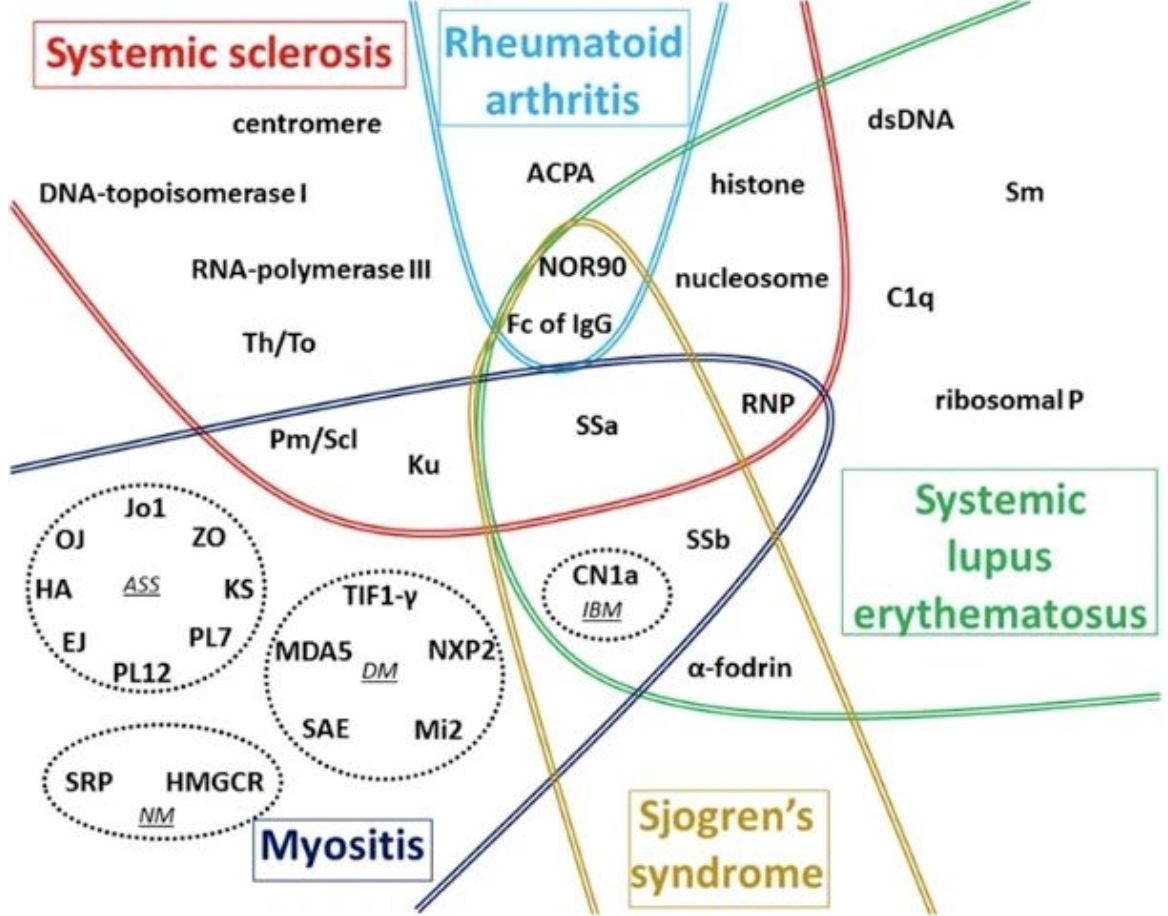
自身免疫性疾病“抗体谱”检测不可忽视
Front Immunol. 2018 Mar 26;9:541.
浅谈应用于自身免疫性疾病检测的多种血清检测方法
截至目前,对于自身抗体的检测,特别是常规检测项目—ANA的检测,间接免疫荧光法(IIFT)一直都被称之为 “金标准”。而对于特异性自身抗体检测,目前市场上不断有新的方法学出现,从经典的免疫印迹法(LIA)、酶联免疫吸附法(ELISA)到化学发光法(CLIA)等。面对如此多样的检测学,临床医师该如何选择?接下来,本文将对以上检测方法进行系统的介绍,为临床实验室进行正确选择提供参考。
间接免疫荧光法
间接免疫荧光技术(IIFT)因其独特的技术优势一直以来都被称为自身抗体检测的“金标准”,是国内外公认的自身抗体筛查首选方法。
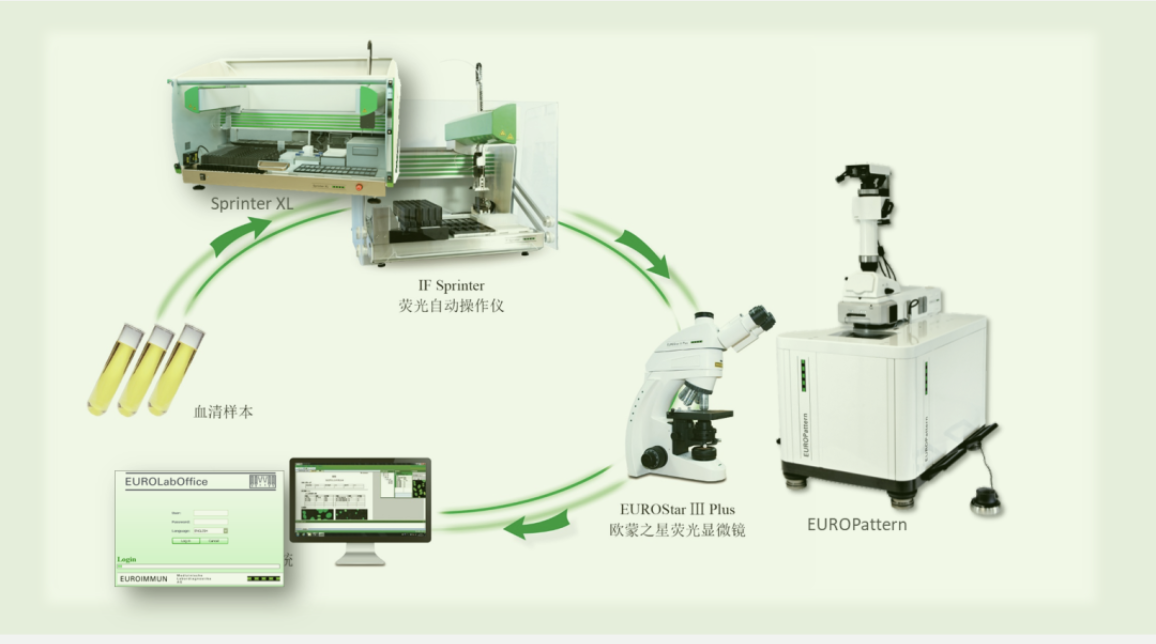
首先,该方法以细胞或组织为检测基质,保留了抗原谱的完整性,保证了自身抗体筛查的敏感性。如HEp-2细胞包含了多达100种靶抗原,可以做到对ANA的全面筛查。同时,以抗原转染细胞为基质的IIFT亦是一种特异性抗体确认方法。该技术将细胞中含量较低的靶抗原以其天然构象大量表达在细胞表面,极大提高了特异性抗体检测的灵敏度和特异性。随着IIFT技术的广泛应用,临床实验室对自动化要求日益迫切,目前欧蒙已经推出了从加样到判读的全自动化IIFT检测平台,大大提升了实验室的工作效率并提高了检测结果判读的标准化。
免疫印迹法
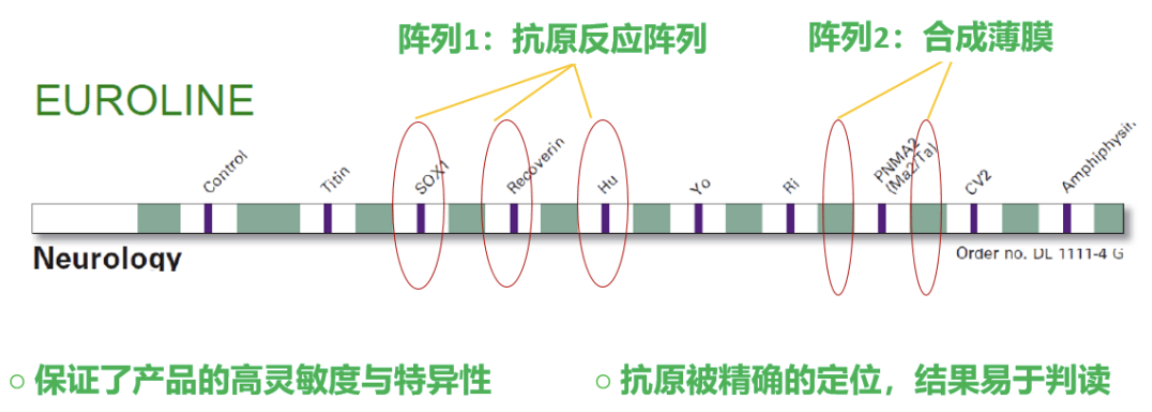
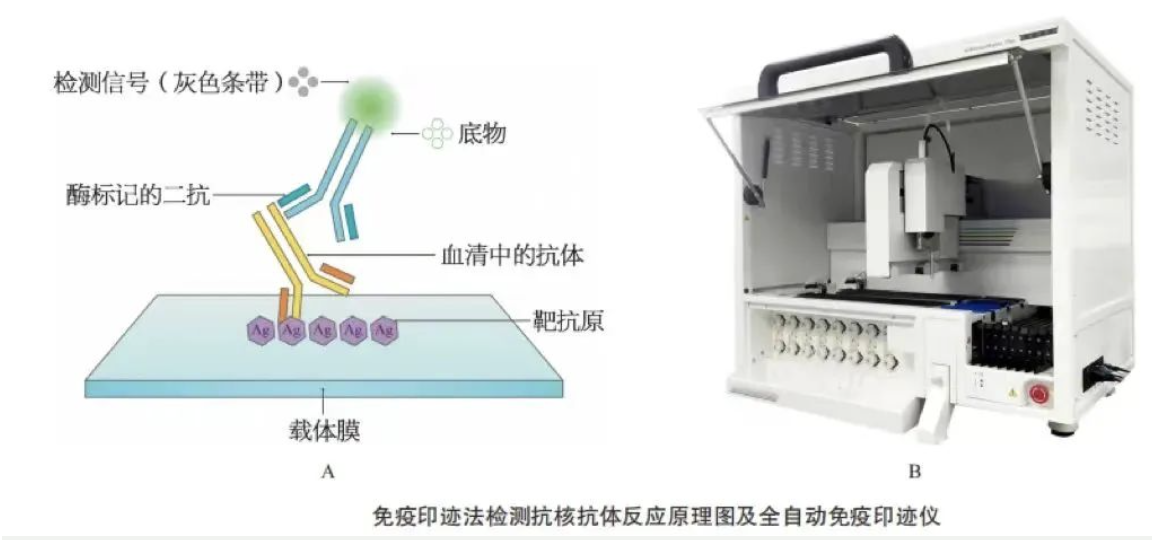
免疫印迹法(LIA)作为多指标联检的特异性抗体确认技术,自90年代初进入中国以来,现已普遍应用于自身抗体检测。该技术是将各种特异性抗原呈条带状包被于理化性质相匹配的不同材质的膜基质上,各种抗原包被带之间间隔一定的距离,由此保证了检测结果的高灵敏和高特异性,并在很大程度上避免了各种抗原间的结果干扰。
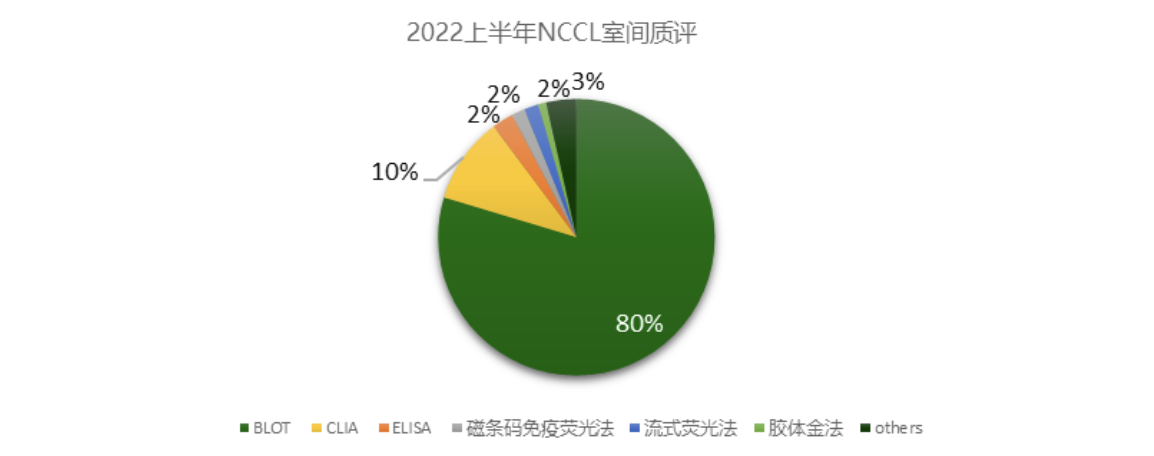
根据2022年国家卫生健康委临床检验中心(NCCL)室间质评上报的1752家实验室数据统计,ENA靶抗原检测的方法学中,使用免疫印迹法的实验室占比80%,是目前自免领域份额占比最大的方法学,且质评结果准确率达到98%,可以看出免疫印迹法使用率很高,备受临床实验室的认可,是自身抗体检测的主流方法学。
免疫印迹法备受青睐,究其原因主要是该技术操作简单、性能优异,多指标联检完全符合临床特异性抗体筛查和确认的需求,经济又高效。此外,免疫印迹法提供的是具有临床意义的半定量检测结果,这种半定量等级结果和抗体水平呈线性相关,且这种相关性已经过长期的临床验证,为临床诊断的把握度和病情的严重程度判断提供了依据。因此,免疫印迹法凭借自身的诸多优势,稳居自身抗体靶抗原确认检测方法中的主导地位。欧蒙配套多种免疫印迹全自动化检测系统,可满足客户的不同诊疗需求。
化学发光法
化学发光法(CLIA)是一种将高特异性的免疫反应和高灵敏度的化学发光测定技术相结合的单指标定量检测技术。该技术根据化学反应产生的辐射光强度来确定物质含量,用于各种抗原、半抗原、抗体、激素、酶、脂肪酸、维生素和药物等的检测。CLIA具有反应速度快、检测灵敏度高、线性范围宽、精密度高,可随到随检等优势。
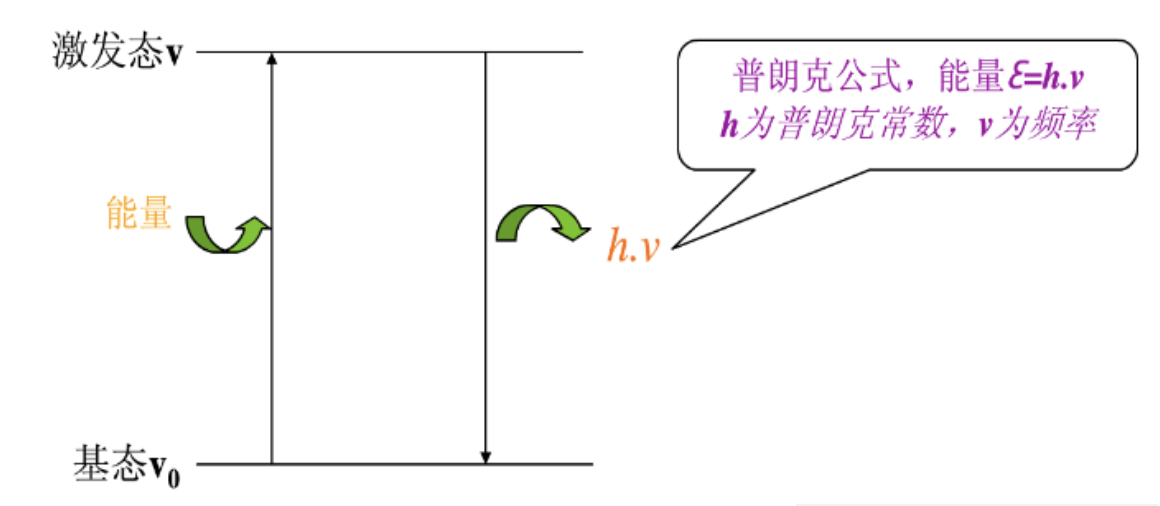
其中,吖啶酯直接化学发光是目前业内较公认的一种高性能检测技术,具有标记物稳定、信号强、背景低、干扰因素少、灵敏度高等诸多优势。如吖啶酯对被标记的抗原、抗体活性无影响,完整保留了抗原抗体的表位活性;吖啶酯光释放快速集中,且发光效率和发光强度均较大;更重要的是,该反应体系无需催化剂和增强剂,只要在H2O2和OH-存在下就能迅速产生化学发光,可以极大的降低背景发光值,提高信噪比。基于此,欧蒙ZETA C21全自动化学发光免疫分析系统就是采用的吖啶酯直接化学发光。ZETA C21检测系统,其检测性能优越,检测项目齐全,与欧蒙其他方法学的检测结果高度匹配,性能稳定,质量有保障。

CLIA近几年被广泛应用于自身抗体检测领域,根据国家风湿病数据中心(CRDC)室间质评数据统计,从2015年到2020年的5年间,使用CLIA检测的实验室不但从无到有,且数量占比大幅上升,如dsDNA和MPO/PR3抗体检测,2020年采用CLIA的实验室占比分别达到14.7%和 22.4%。2022年最新CRDC数据显示,以dsDNA为例,化学发光法从2018年的5.83%上升到了2022年的22.47%。可见CLIA在自身抗体检测领域占有率越来越高。此外,2020年《自身免疫病抗体检测方法的推荐意见》也推荐CLIA用于多种自身抗体的检测,CLIA对自身抗体的定量检测结果能为临床提供更多的参考,符合自身抗体检测的临床需求和发展趋势。同时,因CLIA为单指标检测,可根据疾病临床诊断路径对相应的指标进行单独或组合检测,不必每次进行全套自身抗体谱检测,因此,可以有效降低医保及患者负担,符合DRG/DIP政策的实施。
总结
综上,各种方法学有其各自的优势与短板,自身抗体检测技术的蓬勃发展,为用户带来了更多的选择空间,满足了更多的应用场景。间接免疫荧光法作为经典的自身抗体检测技术,一直以来都有着无法替代的地位。免疫印迹法经历了长期的临床验证,性能已经被广泛认可,在今后很长时间内将依旧是临床主要的自身抗体检测方法。在自身抗体检测领域,化学发光法是全定量检测的代表方法学。由于其是单指标检测,可灵活组合,符合DRG/DIP的医保政策和临床精准检测需求,是今后定量检测需求的不二选择。但是,除了定量检测之外,对于自身免疫性疾病,“抗体谱”的检测仍然不可忽视。面对如此多的检测方法,用户只需从实际使用的需求出发,对方法学进行全面的评估,就能找到最适合自己实验室的检测技术。
自身抗体检测方法学推荐
以ANA为例,对于临床疑似自身免疫性疾病的患者,应同时进行ANA筛查+确认检测。一方面,检测方法的敏感度和特异性相互依存的关系,决定了检测的效能和检测结果的可靠性。另一方面,方法学之间可以相互补充,互相验证,避免漏检,并对假阳性的情况加以甄别,为临床提供准确的辅助诊断结果。
具体推荐的检测策略如下:
